 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电极电势为正值的电极只能作原电池的正极。()
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 如搜索结果不匹配,请联系老师获取答案
如搜索结果不匹配,请联系老师获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“电极电势为正值的电极只能作原电池的正极。()”相关的问题
更多“电极电势为正值的电极只能作原电池的正极。()”相关的问题
第1题
A.在原电池中一定是相对较活泼的金属作负极不活泼的金属作正极
B.在原电池中,电子流出的一极是负极,该电极被还原
C.原电池可以把物质内部的能量全部转化为电能
D.实验室欲快速制取氢气,可利用粗锌与稀硫酸反应
第5题
由标准钴电极(Co2+/Co)与标准氯电极组成原电池,测得其电动势为1.64V,此时钴电极为负极。已知 (Cl2/Cl-)=1.36V。问:(1) 标准钴电极的电极电势为多少(不查表)?(2) 此电池反应的方向如何?(3) 当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化?(4) 当Co2+的浓度降低到0.010mol·dm-3时,原电池的电动势将发生怎样的变化?数值是多少?
(Cl2/Cl-)=1.36V。问:(1) 标准钴电极的电极电势为多少(不查表)?(2) 此电池反应的方向如何?(3) 当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化?(4) 当Co2+的浓度降低到0.010mol·dm-3时,原电池的电动势将发生怎样的变化?数值是多少?
第6题
将下列化学反应写成两个电极反应,查表求出其电极电势值并计算原电池的电动势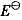 ,再计算电池反应的
,再计算电池反应的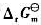 。
。

第8题
A.原电池主要是利用两极的电势差,使电子偏向一方,从而产生电流
B.原电池的电极由两极材料决定,两者相比容易失去电子的一极为负极
C.活泼的一极为负极,另一极则为正极
D.不一定活泼的一极为负极,另一极则为正极,铜铝在浓硝酸中,铜是负极
第9题
A.构成原电池正极和负极的材料必须是金属
B.在原电池中,电子流出的一极是负极,该电极被还原
C.实验室欲快速制取氢气,可利用粗锌与稀硫酸反应
D.原电池可以把物质内部的能量全部转化为电能
第10题
A.无论是否鼓入空气,负极的电极反应式均为Fe-3e-===Fe3+
B.鼓入空气时,每生成1 mol·OH有2 mol电子发生转移
C.不鼓入空气时,正极的电极反应式为H++e-===H·
D.处理含有C2O的污水时,上端开口应关闭